和碳酸钙稀盐酸(碳酸氢钠和稀盐酸)0-12-29 14:04。
化学上学期期末考试试题及答案
可能的相对原子质量:
H1c-12n-14 O-16 Cl-35.5 Ca-40
第一卷(客观题20分)
1.下列变化是化学变化()
A.碾碎矿石b .融化冰雪c .燃烧酒精d .汽油挥发
2.下列实验现象描述不准确的是()
A.细铁丝在氧气中猛烈燃烧,火星四射。
B.一氧化碳燃烧产生蓝色火焰
c、向无色酚酞溶液中通入二氧化碳气体,溶液变红。
D.白磷在空气体中自燃,产生大量白烟。
3.下列测试操作是正确的()
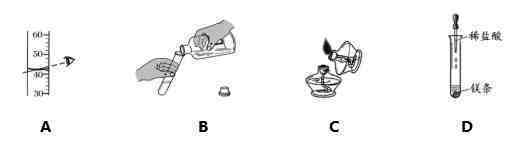
4.钠原子结构示意图如下图所示。关于钠原子不准确的说法是()

A.在化学反应中容易获得电子
B.质子数是11
C.最外层的电子数是1。
D.核心外面有三个电子层。
5.日常生活中,用肥皂水容易起泡的是()。
A.长江水b .矿泉水
C.开水d .含有更多可溶性钙和镁化合物的水
6.苯C6H6是油漆的主要成分之一,是一种常见的化学溶剂,点燃后会产生强烈的黑烟。其反应的化学反应方程式为2c6h 6+XO2 =点火= =12CO2+6H2O。这个反应的化学方程式中x的值是()
A.6 B.9
C.12 D.15
7.下列材料的化学式书写准确的是()
A.碳酸钠NaCO3 B .氢氧化钠Na(OH)2
C.氧化铁3O2Fe D .碳酸H2CO3
8.次氯酸(HClO)具有杀菌消毒的作用,HClO中氯的化合价是()
A.-1 B.+ 1 C.+ 2 D.+ 5
9.餐馆的服务员用盖子熄灭酒精炉。这种灭火方法的重要原理是()
A.切断空气体b .降低温度
C.消除可燃材料d .降低可燃材料的燃点
10.下列推理不准确的是()
(1)燃烧过程伴随着发光和放热,所以发光和放热现象的变化必然是燃烧。
②分子可以构成物质,所以物质必然是由分子构成的。
③单质只含有一种元素,所以含有一种元素的物质一定是单质。
④物理变化中没有新物质产生,所以没有新物质的变化一定是物理变化。
⑤氧化物都含有氧,所以含氧的化合物一定是氧化物。
A.①②③⑤ B.①②⑤ C.①③④ D.③⑤
卷二(主观题40分)
1.(4分)试选:a .钻石,b .二氧化碳,c .二氧化硫,d .盐,e .石墨,f .甲烷,g .活性炭,填以下空白色(填序号字母)
(1)导致温室效应的气体有:
(2)用于刻划玻璃;
(3)天然气的重要成分有:
(4)造成酸雨的重要气体有。
12.(1) (5分)用化学符号表示:
①三个二氧化碳分子;
②两个铜原子;
③碳酸钙中的钙为正二价。
④地壳中最丰富的元素和金属元素形成的化合物;
⑤氯离子;
(2)(6分)水是生命之源,与我们的生活息息相关。
①净水器常用活性炭,应用活性炭很重要。
事业,不仅可以降低水的硬度,而且也是杀菌的方法。
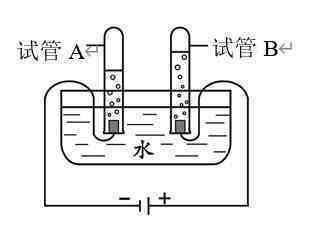
②电解水的装置如右图所示。试管B中的气体是,通过这个试验证明水是由组成的,这个反应的化学方程式是。
13.(6分)下图显示了几种中学常用材料在一定条件下可以转化,A是石灰石的重要成分,E和G是黑色粉末,C是无色液体,H是紫色固体。(部分条件省略)
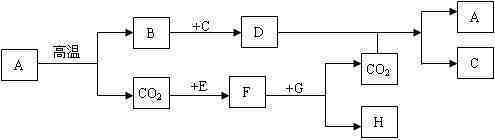
(1)写出下列材料的化学式:A C D E F。
(2)CO2流入D澄清液的化学反应方程式为:
14.(6分)某学习小组围绕“气体实验室准备”进行研究。请参与以下问题。
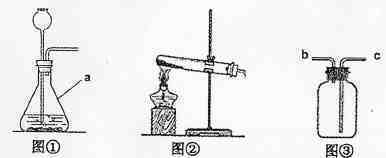
(1)原理分析:实验室中CO2产生的化学方程式如下。
不用Na2CO3和盐酸反应制备CO2的原因是。
(2)发生装置:图①装置中仪表A的名称为。实验室常用无水乙酸钠固体和钠钙在加热条件下生成CH4,应选用绘图(填写序号)发生器。
(技术资源网3)收集装置:实验室收集NH3(易溶于水)应采用的方法如下。收集有毒气体SO2时,常采用③收集装置,气体应从(信)端引入。
15.(7分)达州天然气丰富,有“中国气都”的美誉。甲烷(CH4)是天然气的重要成分。学校化学兴趣小组的同学对甲烷燃烧的产物很感兴趣。请参与:
【提出的问题】:甲烷燃烧后产生哪些技术资源和材料?
【参考资料】:含碳物质完全燃烧生成CO2,不完全燃烧生成CO;无水硫酸铜遇水变蓝。
[假设和设想]:
甲基二氧化碳H2O;乙基H2O;
NH3 CO2 H2O;;H2O二氧化碳公司。
你觉得同学的期望是错的,因为。
【实验探究】:
为了验证上述假设和设想,甲烷在一定量O2中燃烧的产物依次通过以下装置:
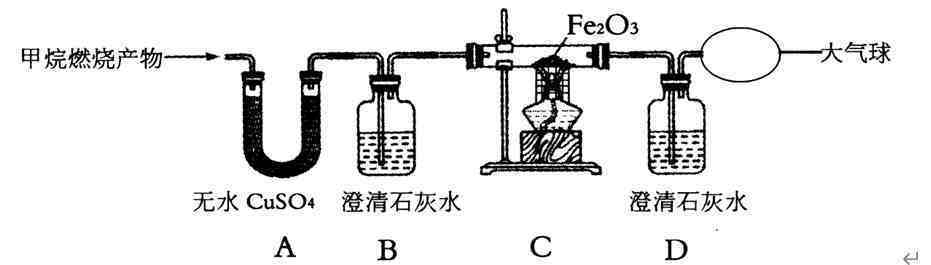
1.设备A和B的顺序可以颠倒吗?(填写“是”或“否”)。
2.实验中观察到A中的无水CuSO4变成蓝色,B和D中的澄清石灰水变成浑浊,C中的中色粉末变成黑色,推断该同学假设成立。
3.请写出C中红色粉末变黑的化学方程式:。
[反思与交流]:
为了避免有毒的CO污染环境,含碳材料燃烧必须满足的条件如下。
在设备D后添加一个大气球的原因是:
16.(6分)黄石市华新水泥厂实验室,为了测定某矿石灰石中碳酸钙的质量分数,取一个石灰石样品和足够的稀盐酸在烧杯中反应(假设石灰石样品中的杂质不与稀盐酸反应,不溶于水。)相关测试数据如下:

(1)根据质量守恒定律,反应生成的二氧化碳质量为g。
(2)求出石灰石中碳酸钙的质量分数。
化学期末论文参考答案
11.(4分)
(1)B、F
(2)答
(3)F
(4)C
12.(1) (5分)
①3 CO2;
②2Cu;
③
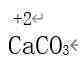
④al2o 3;
⑤Cl–
(2)(6分)
①吸附沸腾
②O2或氧气H、O或氢氧化物
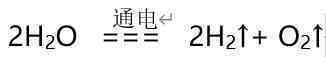
13.(6分)
①A . CaCO3 C . H2O D . Ca(OH)2 E . C F.CO
(2)二氧化碳+氢氧化钙==碳酸钙↓+H2O
14.(6分)
(1) CaCO3+2HCl === CaCl2+H2O+CO2↑
响应速度太快,无法收集气体。
(2)锥形技术资源网瓶,②
(3)下排空集气,c。
15.(7分)
c、不遵循元素守恒(或其他合理答案)
高温
(1)没有
⑵d
(3)3CO+Fe2O3 ==== 2Fe+3CO2
与足够的氧气充分接触。
防止污染空气体
16.(6分)
(1)4.4 (1分)
